در این کلیپ شما با چگونگی نحوه کار با دستگاه HPLC آشنا می شوید.
شیمی تجزیه
شیمی تجزیه به عنوان یک بخش کاربردی در علوم مختلف است هدف از این وبلاگ ارائه روشهای تجزیه ای پرکاربرد است. https://www.instagram.com/_u/ShimiGeramشیمی تجزیه
شیمی تجزیه به عنوان یک بخش کاربردی در علوم مختلف است هدف از این وبلاگ ارائه روشهای تجزیه ای پرکاربرد است. https://www.instagram.com/_u/ShimiGeramترم تابستانی 94
::::::::::::::::::::::ترمی تابستانی hotدر شکوه!!:::::::::::::::::::
::::::::::::::::::::::::::::::::::::::::::::::::::::::::::::::::بفرمایید::::::::::::::::::::::
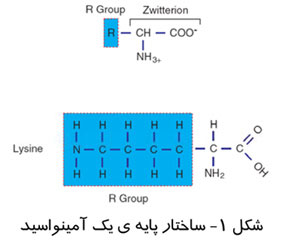
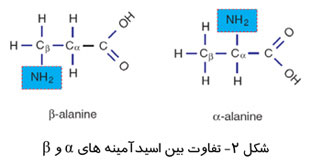
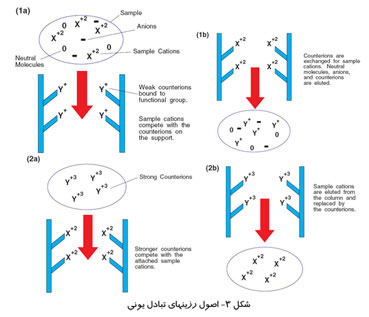
HPLC آمینو اسیدها را آنالیز می کند.

حل تمرین شیمی تجزیه دستگاهی
باسمه تعالی حل تمرین شیمی تجزیه دستگاهی ترم دوم سال 93-92 آزاد تهران جنوب
-عبارتهای ذیل در کروماتوگرافی به چه معنا است؟
-شویش
- فاز ساکن
- زمان بازداری
- ضریب گزینش پذیری
- نفوذ طولی
- تفکیک ستون
- شویش شیبی
- پرکننده نرمال
مساله اصلی شویش در کروماتوگرافی را توضیح دهید؟
تفاوت کروماتوگرافی گاز مایع و مایع مایع را بنویسید؟
چگونه می توان تعداد بشقابک های تئوری یک ستون را بدست آورد؟
چه متغیرهایی بر مقدار ضریب گزینش پذیری برای یک زوج آنالیت تاثیر می گذراند
چرا در منحنی وان دیمتر نقطه کمینه برای HPLC نسبت به GC در سرعت جریان های پایین تر ظاهر می شود؟
متغیرهایی که باعث پهن شدگی کروماتوگرام می شوند را نام ببرید؟
متغیرهایی که باعث جداسازی بهتر کروماتوگرام ها می شوند را نام ببرید؟
تفاوت بین یک ستون لوله مانند باز و یک ستون پرشده را با ذکر معایب و مزایای هر یک بنویسید؟
برنامه ریزی دمایی در کدام روش کروماتوگرافی، و چگونه بکار می رود؟ علت کاربرد آن را شرح دهید؟
چرا از FID بویژه برای نمونه های حاوی آب ، نیتروژن و گوگرد استفاده می شود؟
انواع اجسامی که توسط روش های کروماتوگرافی زیر قابل آنالیز می باشند را بنویسید
- GLC
- GSC
- HPLC
- TLC
چه گونه هایی را می توان توسط HPLC جدا کرد ولی توسط GC قادر به جداسازی آنها نیستیم؟ در صورتی که بخواهیم از GC برای جداسازی آنها استفاده کنیم چه روش آماده سازی نمونه را پیشنهاد می کنید؟
Principles of Reversed Phase Chromatography
بدون شک مهمترین و پرکاربردترین روش جداسازی، روش "کروماتوگرافی" است. کروماتوگرافی (Chromatography)، بوسیله یک گیاه شناس روسی به نام تسوت، در اوایل قرن بیستم (1903) کشف شد. او از این تکنیک برای جداسازی رنگدانه های مختلف گیاهی مانند کلروفیلها و گزانتوفیلها استفاده کرد.
روشهای کروماتوگرافی بر پایه دو مفهوم کلی دسته بندی می شوند: در روش اول، جداسازی بر اساس مفاهیم فیزیکی صورت گرفته و شامل دو گروه کروماتوگرافی ستونی (Column) و کروماتوگرافی سطحی است.
اساس نام گذاری در دسته بندی دوم که مرسوم تر است، نوع فاز متحرک، فاز ساکن و همچنین نوع تعادل ایجاد شده بین دو فاز است. این دسته شامل دو گروه کلی کروماتوگرافی مایع (فاز متحرک مایع می باشد) و کروماتوگرافی گازی (فاز متحرک گاز) است.
2 مفاهیم کلیدی در کروماتوگرافی
درتمامی روشهای کروماتوگرافی، جداسازی بر پایه تفاوت مقداری آنالیت (ماده مورد جداسازی) در دو فاز ساکن (Stationary Phase) و متحرک (Mobile Phase) انجام می شود . این تفاوت مقدار، در نهایت منجر به تشکیل تعادلی می گردد که آن را با پارامتری به نام ثابت توزیع (K) بیان می کنند. در این رابطه Cm و Cs به ترتیب نشان دهنده غلظت مولی آنالیت در فازمتحرک و فاز ساکن است.

نتایج تحقیقات نشان می دهند که پدیده های فیزیکی و شیمیایی متفاوتی بر روی سرعت جداسازی و همچنین پهنای باند دیده شده برای هر آنالیت تاثیر دارند. از بین تئوری های موجود که به توجیه و محاسبه این عوامل می پردازند، تئوری بشقابک های فرضی (Plates) کاربرد بیشتری دارد. در این تئوری فرض می شود که هرستون از یک سری لایه های باریک، افقی وکاملا مجزا از هم، که به طور متوالی قرار گرفته اند، تشکیل شده است. به هر یک از این لایه ها، بشقابک گفته می شود. در هرکدام از این بشقابکها آنالیت در تعادلی بین فاز متحرک و ساکن قرار دارد و در نهایت با انتقال بین بشقابکها عمل جداسازی صورت می پذیرد. کارایی هر ستون به تعداد بشقابکهای موجود درستون و یا به عبارت دیگر به تعداد تعادل های ایجاد شده در ستون بستگی دارد. بنابراین برای بررسی کارایی ستون تعداد بشقابک های فرض (N)را از رابطه زیرمحاسبه می کنند. در این رابطه H نشان دهنده ی ارتفاع هر بشقابک و L طول ستون را به نمایش می گذارد.

3 کروماتوگرافی مایع با کارایی بالا
از میان تکنیک های جداسازی، کروماتوگرافی مایع با کارایی بالا (High Performance Liquid Chromatography -HPLC)، بیشترین رشد و کارایی را داشته است و سالیانه میلیونها دلار صرف خرید و فروش دستگاههای HPLC در دنیا می شود. علت این رشد را می توان به حساسیت بالا، تعیین مقدار کمی با صحت بالا، قابلیت آنالیز نمونه های غیرفرار و حساس به دما که با تکنیکGC (کروماتوگرافی گازی) امکانپذیر نیستند، نسبت داد.
3-1 فاز ساکن و فاز متحرک
در مورد قطبیت فازهای ساکن و متحرک یک قاعده کلی وجود دارد. طبق این قاعده، قطبیت حل شونده و فاز متحرک باید نزدیک به هم باشد، ولی با فاز ساکن اختلاف داشته باشد. ترتیب قطبیت گروههای عاملی در ترکیبات به صورت زیر است:
هیدروکربن < اترها < استرها < کتونها < آلدئیدها < آمیدها < آمینها < الکلها
خصوصیات فاز متحرک در HPLC در زیر آمده است:
• درصد خلوص بالا ( حلالهایی با درصد خلوص بسیار بالا ، HPLC Grade، در بازار موجود است که قیمت بالایی نیز دارد.)
• نقطه جوش بالاتر از دمای ستون ( به خصوص در مواردی که با گرمکن (Oven) کار می شود)
• واکنش پذیری کم (Inertness)
• قابلیت تطابق با آشکارساز
3-2 اجزاء و قسمتهای مختلف دستگاه HPLC
دستگاه و تجهیزات HPLC شامل قسمت های مختلفی است که در ادامه به آنها اشاره می شود:
1- مخازن حلال: که در آنها فاز متحرک و یا حلالهای شستشو دهنده ستون ریخته شده است.
2- موتور یا پمپ: به منظور انتقال حلال و همچنین نمونه در فضای نسبتا طویل ستون نیاز به ایجاد فشاری در سیستم است که برای ایجاد آن حداقل از یک پمپ یا موتور استفاده می شود. حلال (فاز متحرک) توسط پمپ با سرعت و جریان ثابتی بر روی فاز ساکن حرکت داده می شود. فشار سیستم به اندازه (سایز) ذرات موجود در ستون، گرانروی (Viscosity) و سرعت جریان فاز متحرک بستگی دارد. بسته به نوع جداسازی، میزان سرعت جریان فاز متحرک تعیین می گردد. در مواردی که با تعددی از آنالیتها مواجه هستیم، هر گونه جدا شده خود را به صورت یک پیک در کروماتوگرام نهایی نشان میدهد. در سرعت جریان کمتر فاز متحرک ، فاصله بین پیک ها افزایش یافته و جداسازی بهتری خواهیم داشت. معمولا گفته می شود که در ستون هایی با قطر مرسوم (کمتر از 5mm) سرعت جریان نباید بالاتر از 2/5 ml/min باشد چرا که باعث صدمه زدن به ستون و کاهش عمر مفید آن می شود.
به عنوان فاز متحرک، مخلوطی از حلالها در ازای یک حلال خالص میتواند بهکار گرفته شود. نسبت اجزاء فاز متحرک در طی یک تزریق ممکن است ثابت باشد که در این صورت به آن روش ایزوکراتیک (Isocratic) گفته می شود. در حالتی دیگر که به آن روش گرادیانت ) ( Gradient گفته می شود، طی یک تزریق و با پیشرفت زمان، طبق برنامه ای که از قبل برای سیستم تعریف شده است، درصد متفاوتی از دو یا چند حلال مخلوط شده و در سیستم توسط پمپ جریان می یابد.
3- تزریق کننده(Injector): تزریق نمونه، بسته به نوع دستگاه، به دو شکل دستی و یا خودکار انجام می گیرد. در روش خودکار، نمونه در ظروف مخصوصی ریخته شده و در محل تعبیه شده در دستگاه قرار می گیرد. پس از اینکه اپراتور دستور تزریق را (از طریق نرم افزار ) می دهد، نمونه توسط یک سرنگ به سیستم منتقل می شود. در روش دستی، از سرنگ هایی با ظرفیت های مختلف برای تزریق نمونه استفاده می شود. حجم نمونه تزریق شده (در هر دو روش)، به حجم حلقه نمونه بردار ( Loop )بستگی دارد و مقدار آن معمولا در حد 5 تا 500 میکرولیتر است. نمونه ابتدا وارد این حلقه شده و پس ازآماده شدن سیستم به همراه فاز متحرک وارد ستون می شود.
4- ستون: پس از تزریق، نمونه ابتدا وارد قسمتی به نام پیش ستون (pre-column) یا ستون محافظ (Guard column ) می شود. نقش این ستون محافظت از ستون اصلی است. طول این ستون معمولا در حد سانتی متر است و جنس آن از فولاد ضد زنگ است. ماده پرکننده (Packing) ستون محافظ از جنسی مشابه ماده پرکننده ستون اصلی است. هم جنس بودن نوع پرکننده این مزیت را دارد که اگر ماده ای که با ذرات ستون وارد واکنش شود در نمونه موجود باشد، در ابتدا در ستون محافظ به دام افتاده وستون اصلی را دچار آسیب نمی کند. طول ستونهای اصلی دستگاه معمولا حدود 30-10 سانتی متر بوده و درون ستون را با موادی که به یکی از دو فرم پوسته دار و یا متخلخل است، پر کرده اند. سایز این مواد پرکننده که بر کیفیت جداسازی تاثیر فراوانی دارد متفاوت بوده و معمولا در حد 3 تا 5 میکرومتر است.
ستون می تواند قطبی و یا غیرقطبی باشد. از مرسوم ترین ستون های غیرقطبی میتوان به C18، اکتادسیل سیلان ODS)) اشاره کرد. جنس ستونها از فولاد ضد زنگ (Stainless Steel) است. پس از ورود نمونه به ستون، بر اساس تفاوت قطبیت، اجزاء مختلف نمونه در زمان های متفاوتی با نام زمان بازداری (Retention Time) از یکدیگر جدا شده و برای تشخیص نوع ماده به سمت آشکار ساز(Detector) هدایت می شوند.
در نهایت پس از اتمام کار باید ستون را شستشو دهیم. برای شستشو، بسته به نوع ستون، حلال متفاوتی را با ترتیب خاص انتخاب می کنیم. برای مثال در ستون های غیرقطبی پس از اتمام کار، ابتدا ستون را با یک حلال قطبی (معمولا آب ) و سپس با یک حلال غیرقطبی (معمولا متانول) شستشو می دهند.
5- آشکارساز (Detector): آشکارساز بر اساس نوع آنالیت انتخاب می شود. به طور کل یک آشکارساز خوب باید دارای ویژگی های زیر باشد:
> حساسیت بالا
> غیرتخریبی بودن (Nondestructive): در طول روند شناسایی نمونه را تخریب نکند.
> پاسخ خطی به غلظت در دامنه وسیع (برای سهولت در محاسبات)
درادامه به تعدادی ازآشکارسازهای مرسوم اشاره می شود :
الف- از پر کاربردترین انواع آشکارساز،طیفسنج UV-Vis است که برای اجسامی که در این ناحیه جذب داشته باشند مورد استفاده قرار می گیرد. در این آشکارساز با استفاده از تفاوت میزان جذب نمونه با منبع نوری اولیه و در نهایت با استفاده از قانون بیر لامبرت غلظت نمونه اندازه گیری می شود. در مواردی که از این آشکارساز استفاده می شود انتخاب طول موج مناسب یکی از مواردی است که می بایست مد نظر قرار بگیرد، در طول موج انتخابی، نباید مزاحم های موجود در نمونه و همچنین حلال جذب داشته باشند.
ب- آشکارساز ضریب شکست، اساس کار این آشکارساز بر مبنای تغییراتی است که در ضریب شکست سیستم حلال به تنهایی و سیستم حلال همراه با نمونه، ایجاد می شود.پاسخ این آشکارساز به حرارت وابسته بوده و به همین دلیل معمولا به ندرت ازآن استفاده می-شود.
ج- آشکارساز فلورسانس، حساس تر از آشکارساز UV/Vis است ولی ترکیبات کمی موجودند که خاصیت فلورسانس داشته باشند درنتیجه کاربرد این آشکارساز نیز محدود است.
د- آشکارساز الکتروشیمیایی، که عملکرد آن بر پایه واکنش های اکسید و احیا می باشد و شامل روشهای آمپرومتری (Amperometry)، پلاروگرافی(Polarography)، کلون سنجی (Coulometry) و هدایتسنجی (Conductometry) است.
ه- آشکارساز طیف سنج جرمی (MS): این مورد امروزه به دلیل مزایای زیادی که دارد به طور وسیعی مورد استفاده قرار می گیرد.از این جمله میتوان به حد تشخیص (LOD) بسیار پایین، حساسیت و انتخابگری (Selectivity) بالاو امکان بررسی نمونه در حضور مزاحمهای شیمیایی اشاره کرد.
در صورتیکه از هیچ کدام از این موارد نتوان استفاده کرد، از مشتق سازی (ایجاد تغییرات شیمیایی روی نمونه) جهت ایجاد نمونه فعال در هر یک از این آشکارسازهای ذکر شده استفاده می شود. شکل زیر نمایی از یک دستگاه HPLC را به همراه اجزاء مختلف آن به تصویر کشیده است] [.

یک نمونه کروماتوگرام در شکل 2 نشان داده شده است که در آن سه نوع قند از یکدیگر جدا شده اند. اطلاعات کمی، نیمه کمی و کیفی از ولتاموگرام قابل استخراج است.

آنالیز کیفی، برای تشخیص و شناسایی نوع ترکیبات انجام می شود. از آنجایی که زمان بازداری (Retention Time) برای هر ماده در یک سیستم و شرایط خاص آزمایشگاهی ثابت و مشخص می باشد، می توان از آن جهت تعیین نوع آنالیت استفاده کرد. به این منظور کروماتوگرام آنالیت را با کروماتوگرام به دست آمده از استاندارد آن آنالیت مقایسه می کنند. در صورت یکسان بودن زمان بازداری می توان با قطعیت نوع ماده را تعیین کرد. ذکر این نکته لازم است که این مقایسه این دو کروماتوگرام تنها در شرایط آزمایشگاهی و دستگاهی کاملاً یکسان معتبر است.
4-2 آنالیز کمی:
به منظور تعیین کمی مقدار آنالیت، سطح زیر پیک و یا ارتفاع پیک ترکیب مجهول را با نمونه استاندارد مقایسه می¬کنند. در مواردی که پیک ها باریک و متقارن باشند، اندازه گیری ارتفاع پیک از صحت و سرعت بیشتری برخوردار است. هر چند که امروزه به راحتی می توان ارتفاع و سطح زیر پیک را به کمک دستگاه های الکترونیک با دقت و صحت بالایی محاسبه کرد. روشهای مختلفی جهت محاسبه مقدار مجهول وجود دارد که در ادامه به برخی از این روشها اشاره می شود:
4-2-1 روش استاندارد خارجی (External Standard):
در این روش، محلولهایی با غلظت های مختلف از استاندارد (استاندارد آنالیت مورد نظر) ساخته شده و سپس بر اساس ارتفاع یا سطح زیر پیک بدست آمده از کروماتوگرام این استانداردها، منحنی کالیبراسیون ( منحنی ارتفاع و یا سطح زیر پیک، بر حسب غلظت) رسم می شود. با استفاده از معادله خط بدست آمده، مقدار ارتفاع و یا سطح زیر پیک نمونه مجهول، مقدار دقیق آنالیت محاسبه می شود.
4-2-2 روش افزایش استاندارد (Standard Addition):
در این روش ابتدا ماده مجهول، آنالیز می شود، سپس به چند ظرف که حاوی مقدار یکسانی از نمونه است، حجم های مشخصی از استاندارد اضافه می شود و کروماتوگرام مربوط به هر مرحله را آنالیز و در نهایت ارتفاع یا سطح زیر پیک نمونه ها را بر اساس حجم استاندارد اضافه شده رسم می کنند. در نهایت با استفاده از روابط موجود می توان غلظت نمونه را محاسبه کرد. استفاده از این روش سبب حفظ بافت و ماتریس نمونه ها می شود در نتیجه با این روش احتمال مزاحمت بافت (Matrix Interference) نمونه از بین برده می شود.] [
4-2-3 استاندارد داخلی (Internal Standard):
دو نوع خطا (سیستماتیک و تصادفی) در سیستم موجود است. برخی از این منابع ثابت را می توان با اضافه کردن یک استاندارد داخلی به نمونه ها و تقسیم ارتفاع پیک یا سطح زیر پیک مربوط به هر آنالیت بر همین مقادیر مربوط به استاندارد داخلی، حذف کرد. در انتخاب استاندارد داخلی باید به شباهت های ساختاری آنالیت با جزء انتخابی، نزدیک بودن زمان بازداری پیک آن به پیک نمونه و ..، توجه کرد. با انتخاب یک استاندارد داخلی مناسب می توان خطا را از 1 تا 2 درصد به 5.0 تا 1 درصد کاهش داد.
5- نتیجه گیری:
کروماتوگرافی مایع با کارایی بالا، روشی مناسب جهت جداسازی، اندازه گیری، و تعیین نوع مواد است. این تکنیک با تلفیق با روشهای دیگر و آشکارسازهای پیشرفته ای مانند طیف سنج جرمی کاربرد های زیادی در علوم مختلف دارد. انتخاب فاز متحرک و ثابت، انتخاب آشکارساز و تعیین سرعت جریان فاز متحرک از جمله موارد اساسی در تنظیمات یک روش مناسب HPLC است.
منابـــــع :
- 1. Skoog, D.A. "Principle of Instrumental Analysis", 3nd Edition, USA: Saunders College Publishing, (1985).
- 2. Rouessac, F, Rouessac, A. "Chemical Analysis Modern Instrumentation Methods and Techniques" 2nd Edition, England, John Wiley & Sons Ltd, (2007).
- 3. اسگوگ، هالر، نیمن، "اصول تجزیه دستگاهی" ترجمه: عبدالرضا سلاجقه، چاپ اول، تهران، مرکز نشر دانشگاهی،جلد اول (1382)
اطلاعیه
سلام
به اطلاع دانشجویان درس شیمی تجزیه 1 و درس شیمی تجزیه دستگاهی می رسانم مطابق اعلام قبلی این دروس ساعت 8 تا 10 به ترتیب در روزهای یکشنبه و سه شنبه برگزار خواهد شد هر گونه تاخیر در این کلاس ها به منزله غیبت تلقی خواهد شد.
پی نوشت:
کلاس بدون تنفس درسی (آنتراک) و پیوسته خواهد بود.
معرفی روش میکرو استخراج با استفاده از فیبر تو خالی
سلام
روش های میکرو استخراج یکی از پرکاربردترین روشهای پیش تغلیظ و استخراج است. یکی از این روش ها بر پایه استفاده از فیبر توخالی می باشد که نقش فیبر توخالی نگه داری حلال میکرواستخراج و افزایش سطح تماس آن برای انتقال آنالیت یا آنالیت ها از محلول به میکروحلال است.
هر گونه اقتباس از این مبحث با ذکر منبع این وبلاگ بلامانع است.
